
2025年11月6日,重庆医科大学信息与肿瘤免疫研究院张泽民院士团队联合深圳湾实验室、北京大学、中山大学肿瘤防治中心和基因组多维解析技术全国重点实验室等合作团队在Cancer Cell期刊在线发表题为Remodeling of T and endothelial cells during total neoadjuvant therapy in rectal cancer的研究论文。该研究通过多维度技术手段,系统解析了TNT对局部晚期直肠癌(locally advanced rectal cancer, LARC)肿瘤免疫微环境的重塑,揭示CD8+T细胞与内皮细胞的相互作用是TNT发挥临床疗效的潜在重要原因。这一成果为提升直肠癌治疗疗效、优化临床诊疗方案提供了新视角,有助于我们对直肠癌新辅助治疗领域复杂机制的理解。

结直肠癌是全球高发的消化道恶性肿瘤,其发病率与致死率分别位居全球恶性肿瘤第三位、第二位,严重威胁人类健康。其中约85%的结直肠癌患者具有微卫星稳定性及成熟错配修复能力(proficient mismatch repair, pMMR),该类患者肿瘤突变负荷低、免疫原性弱,对当前主流的免疫检查点抑制剂治疗响应率较低。因此,新辅助放化疗成为该类患者的推荐治疗方案,而能进一步提升患者完全响应率的全程新辅助治疗(total neoadjuvant therapy, TNT),其具体作用机制(尤其在单细胞层面如何影响免疫组分与细胞相互作用)此前尚未明确,成为临床转化与疗效优化的关键瓶颈。
2025年11月6日,重庆医科大学信息与肿瘤免疫研究院张泽民院士团队联合深圳湾实验室、北京大学、中山大学肿瘤防治中心和基因组多维解析技术全国重点实验室等合作团队在Cancer Cell期刊在线发表题为Remodeling of T and endothelial cells during total neoadjuvant therapy in rectal cancer的研究论文。该研究通过多维度技术手段,系统解析了TNT对局部晚期直肠癌(locally advanced rectal cancer, LARC)肿瘤免疫微环境的重塑,揭示CD8+T细胞与内皮细胞的相互作用是TNT发挥临床疗效的潜在重要原因。这一成果为提升直肠癌治疗疗效、优化临床诊疗方案提供了新视角,有助于我们对直肠癌新辅助治疗领域复杂机制的理解。
针对这一问题,研究团队对26例LARC患者治疗前后的组织样本及血液样本(共 92 例)开展系统性研究,综合运用单细胞测序、单细胞 T 细胞受体(TCR)测序、空间转录组测序等前沿技术,结合多色免疫荧光实验、体外功能验证实验及配对样本动态分析,构建了TNT治疗前后肿瘤免疫微环境的动态变化图谱,首次阐明CD8+T细胞与内皮细胞的相互作用可能是TNT发挥临床疗效的核心机制。
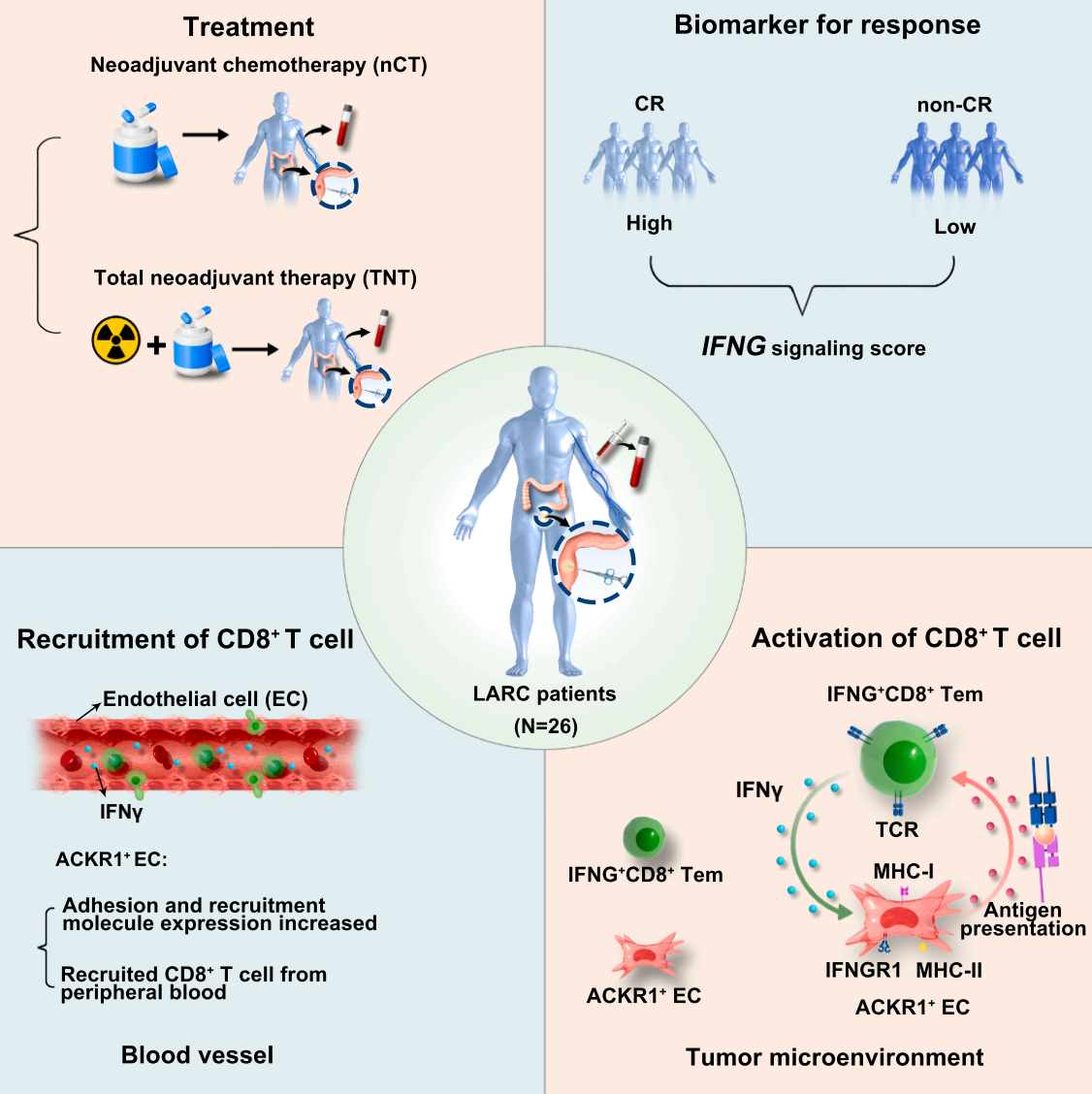
研究团队通过对比分析新辅助化疗(neoadjuvant chemotherapy, nCT)、中间时间点新辅助放疗(neoadjuvant radiotherapy, nRT)与TNT三种治疗方案的效果,得出多项重要结论:
TNT显著强化抗肿瘤免疫应答:相较于nCT与nRT,TNT可显著提升肿瘤组织中IFNG+CD8+T细胞(具有强抗肿瘤活性的 T 细胞亚群)的浸润比例,同时上调肿瘤免疫微环境中IFNG及其相关信号通路的表达水平;更重要的是,TNT能系统性增强患者外周血中的IFNG信号强度,且该信号强度可作为区分患者是否达到 “完全响应” 的潜在临床生物标志物,为临床疗效预判提供了便捷、可靠的检测指标。
内皮细胞亚群为免疫招募关键 “桥梁”:研究首次发现内皮细胞(endothelial cells, ECs)中的ACKR1+ECs亚群,是招募外周血中CD8+T 细胞进入肿瘤微环境的重要 “载体”。进一步研究表明,TNT治疗后,ACKR1+ECs不仅招募能力增强,还呈现出抗原递呈功能与 T 细胞激活能力显著提升的特征;体外实验证实,ACKR1+ECs对CD8+T细胞的激活具有抗原特异性,确保免疫应答的精准性。
细胞间作用闭环强化杀伤效果:TNT治疗后,ACKR1+ECs的IFNG信号通路及IFNγ受体(IFNGR)表达水平显著上升,提示其功能受IFNG+CD8+T细胞分泌的IFNγ调控;二者形成 “IFNG+CD8+T细胞→调控ACKR1+ECs→招募并激活更多CD8+T细胞” 的作用闭环,持续放大抗肿瘤免疫效应,最终提升肿瘤杀伤效率。
综上所述,本研究系统性地阐释了全程新辅助治疗对局部晚期结直肠癌患者肿瘤免疫微环境的重塑作用,揭示了患者潜在响应机制,并开发了预测患者响应完全与否的生物学标志物,具有一定的基础研究与临床转化价值。
该研究由多领域科研团队协同完成。该课题起步于深圳湾实验室肿瘤研究所,最终由科研团队在重庆医科大学完成,深圳湾实验室为该课题提供了重要支持。重庆医科大学/北京大学BIOPIC张泽民院士、中山大学肿瘤防治中心丁培荣主任、北京大学BIOPIC朱琳楠副研究员(原深圳湾实验室副研究员)、重庆医科大学程斯进教授及高千千教授为共同通讯作者;重庆医科大学高千千教授(原深圳湾实验室副研究员)、北京大学博士生凌心楠、中山大学肿瘤防治中心廖乐恩博士、北京大学博士后唐非、基因组多维解析技术全国重点实验室&杭州华大生命科学研究院姜宇佳博士为共同第一作者。
原文信息:
Remodeling of T and endothelial cells during total neoadjuvant therapy in rectal cancer
文章来源|BioArt
编辑|鲍 鲍
责编|远 山
欢迎投稿、建议|media@szbl.ac.cn

 粤公网安备44031102000926号
粤公网安备44031102000926号