免疫检查点阻断疗法,特别是PD-L1阻断疗法,通过中断PD-L1/ PD-1信号通路能有效恢复抗肿瘤适应性T细胞免疫反应,在临床上取得了初步成功。然而PD-L1阻断疗法仍然存在客观响应率低和潜在的全身副作用等挑战。研究表明,癌细胞不仅通过适应性免疫效应来抵抗宿主的免疫反应,还依赖于先天免疫,特别是肿瘤细胞上的CD47通过与巨噬细胞的SIRPα相互作用保护其免受巨噬细胞的吞噬。
近年来,得益于其优异的生物安全性和稳定性,细胞膜囊泡被广泛应用于药物递送和癌症免疫治疗。在前期研究的基础上,深圳湾实验室饶浪团队与新加坡国立大学陈小元等团队合作,开发了一种基因可程序化的融合细胞膜囊泡,同时表达SIRPα变体和PD-1,用于双靶向免疫检查点阻断治疗。
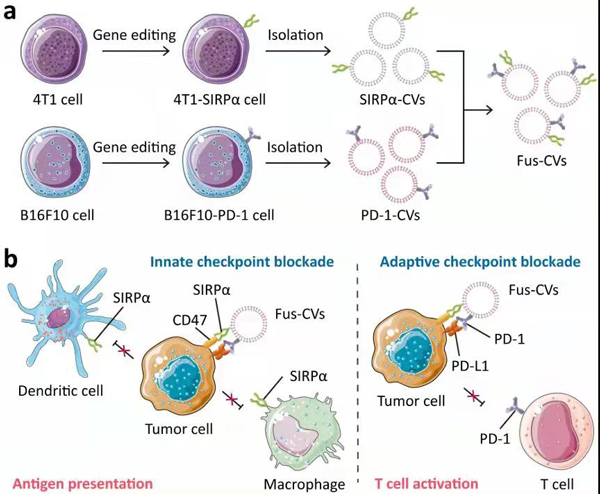
通过融合单个基因编辑的细胞膜囊泡,融合细胞膜囊泡同时高表达SIRPα和PD-1。利用融合细胞膜囊泡双靶点阻断固有检查点CD47和自适应检查点PD-L1,可以显著促进巨噬细胞和树突状细胞(DCs)的抗原提呈,并引发抗肿瘤T细胞免疫应答。此外,融合细胞膜囊泡的的双特异性靶向设计确保了对肿瘤细胞的靶向性较好,而对其他细胞的靶向性较低,有效降低了全身副作用,提高了治疗效果。
实验结果表明,该融合细胞膜囊泡能有效地促进巨噬细胞对肿瘤细胞的吞噬作用。在4T1小鼠模型中,研究者观察到CD11c+细胞显著增加,这些细胞显示出CD80和CD86高表达,表明它们的成熟状态和促进抗原提呈的能力。同时,调节性T细胞(Treg)和髓源抑制细胞(MDSCs)的减少揭示了肿瘤免疫抑制微环境的逆转,有效促进了T细胞激活。进一步在小鼠模型上验证了该融合细胞膜囊泡的抗肿瘤效果。此外,双靶标设计保证了该融合细胞囊泡靶向肿瘤,而减少与其它细胞的相互作用,有效抑制了肿瘤生长。
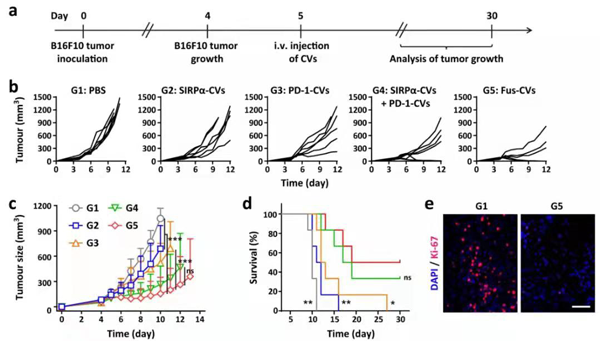
综上所述,本文设计了一个基因可程序化的融合细胞膜囊泡,通过同时表达SIRPα变体和PD-1,用于增强肿瘤免疫治疗,为多靶点的免疫检查点治疗提供了新思考。
原文信息:
Genetically Programmable Fusion Cellular Vesicles for Cancer Immunotherapy
文章来源 | WileyChem
编辑 | 鲍 啦