6月10日,深圳湾实验室坪山生物医药研发转化中心(以下简称“坪山中心”)/北京大学深圳研究生院李子刚教授和伦敦大学玛丽女王学院John Viles教授合作在The FEBS Journal杂志上发表了题为“Therapeutic potential for amyloid surface inhibitor: Only Amyloid-β oligomers formed by secondary nucleation disrupt lipid membrane integrity”的文章。
阿尔茨海默病的特征之一是细胞外β-淀粉样蛋白(Aβ)的异常积累。Aβ单体可以聚集成可溶性的寡聚体,并最终形成不溶性纤维。在Aβ聚集体中,寡聚体的神经毒性最强。在大脑中,Aβ与富含脂质体的环境密切相关。脂质体可以影响Aβ的聚集,同时Aβ能够破坏脂质体膜的完整性,并导致细胞稳态的丧失。特异性抑制Aβ毒性寡聚体的产生是治疗阿尔茨海默病的一种有前景的治疗策略。
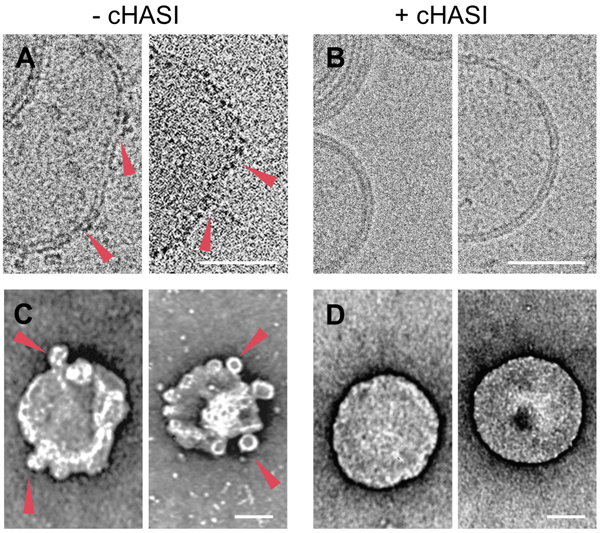
课题组前期合理设计了一种可以特异性抑制Aβ单体与纤维表面结合,从而抑制毒性聚集通路(二级成核)的α-螺旋多肽抑制剂(cyclic helical amyloid surface inhibitor, cHASI)。在本项工作中,作者应用这种多肽抑制剂成功证明在脂质体存在的情况下,cHASI能有效地特异性抑制Aβ的二级成核过程。通过将Aβ单体与脂质体囊泡一起孵育,发现在Aβ组装成淀粉样蛋白纤维的过程中,会产生能够显著破坏脂质体膜的寡聚体。而在cHASI多肽抑制剂存在时,尽管Aβ仍能通过初级成核和伸长过程形成淀粉样蛋白纤维,但是这两种形成原纤维的途径并不会破坏脂质体膜的完整性。这一结果表明只有在二次成核过程中产生的寡聚物才能够破坏膜的完整性。细胞实验进一步证实了cHASI降低Aβ细胞毒性的效果。
本研究证实了抑制Aβ聚集过程中能够大量产生寡聚体的二次成核途径的重要性,为研发淀粉样蛋白抑制剂提供了新的思考方向。
以上工作由坪山中心/北京大学深圳研究生院李子刚教授和伦敦大学玛丽女王学院John Viles教授共同指导完成。伦敦大学玛丽女王学院博士生田瑶和坪山中心刘健博共同完成实验部分。北京大学深圳研究生院博士生杨发灯,坪山中心廉晨珊,南方科技大学副研究员张华威亦对本文做出了重要贡献。以上工作得到了国家自然科学基金委员会、北京分子科学国家研究中心开放资助和深港脑科学研究院-深圳基础研究机构的支持。
原文信息:
文章来源 | 坪山中心
编辑 | 鲍 啦
欢迎投稿、建议 | media@szbl.ac.cn