近日,深圳湾实验室的唐啸宇研究员及中科院深圳先进技术研究院合成生物学研究所的罗小舟研究员在National Science Review(《国家科学评论》)上发表了一篇回顾 “合成生物学生产天然产物” 的评论文章,在该篇评论当中,研究人员分别列举了 3 个代表性案例来介绍合成生物学在天然产物及其衍生物全合成领域的应用,并对其和全合成领域的前景进行了展望。
因为结构的复杂性,天然产物(NPs)一直以来都吸引着化学家们的研究兴趣。更重要的是,进化赋予了其与生物大分子(如核酸、蛋白质和脂质)相互作用的能力,这使得它们成为了药物发现的优势骨架。到目前为止,有超过 50% 的临床批准药物是直接来自天然产物或其衍生物。
然而,难以从天然来源中直接获取足够的原料,已经成为了制约当前天然产物新药开发的主要挑战。尽管合成化学发展至今,有机化学家已经可以合成几乎所有类型的天然产物,但是要实现在合理的成本和时间范围内的全合成生产,对于大多数天然产物来说,仍然十分困难。
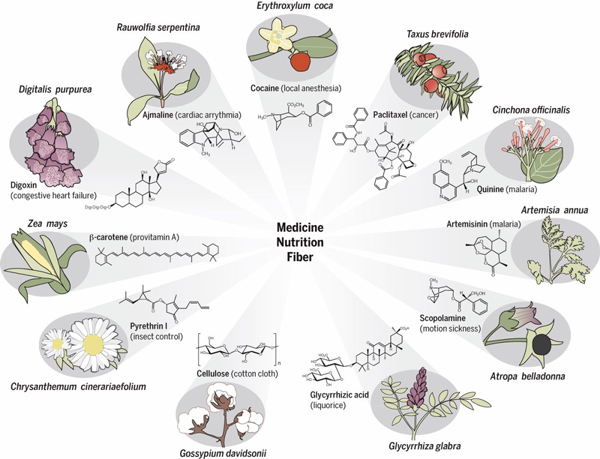
天然产物(来源:Science)
而合成生物学的出现与发展,为这些复杂小分子的经济性生产,带来了希望。因为在自然界中,这些产物本质上便是由基因编码和生物合成的,而在过去的几十年中,人们在揭示天然产物的生物合成上所做出的巨大努力,正为如今利用合成生物技术合成天然产物奠定了基础。
2022 年 8 月 26 日,在National Science Review(《国家科学评论》)上发表了一篇回顾 “合成生物学生产天然产物” 的评论文章,文章的通讯作者为深圳湾实验室的唐啸宇研究员及中科院深圳先进技术研究院合成生物学研究所的罗小舟研究员。在该篇评论当中,研究人员分别列举了 3 个代表性案例来介绍合成生物学在天然产物及其衍生物全合成领域的应用,并对其和全合成领域的前景进行了展望。
第一个例子,是来自链霉菌的抑菌天然产物促肠活动素(Enterocin),其最早是于 1976 年被研究人员所分离和报道,是一个具有三环笼状骨架的聚酮类化合物,对于革兰氏阳性菌和革兰氏阴性菌均具有抑制活性。
长期以来,研究人员都在致力于利用化学或者生物手段对其进行合成。最终,经过十多年的研究攻关,时任亚利桑那大学副教授的 Bradley S Moore 及其同事终于成功揭示了促肠活动素的生物合成途径。
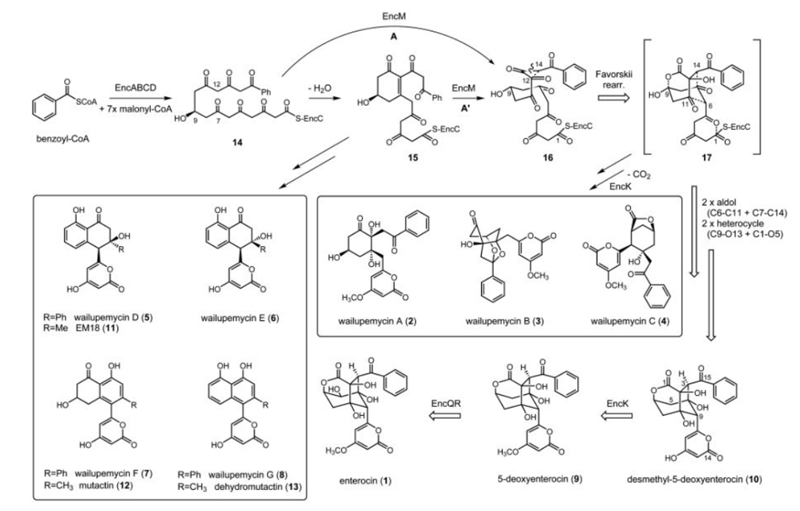
促肠活动素的生物合成途径(来源:PNAS)
基于此,Bradley S Moore 在 2007 年带领团队更进了一步:其通过生物合成酶,成功在体外实现了促肠活动素首次酶促全合成,总产率约为 25%。而该项研究,也是在复杂天然产物上首次实现的全酶合成。
除此之外,促肠活动素生物合成的成功所带来的经验,还最终驱动了该分子的第一个化学全合成的发展。2021 年,来自慕尼黑工业大学的 Thorsten Bach 团队便利用仿生策略,成功实现了从 L - 阿拉伯糖开始共 22 步 0.4% 总产率的促肠活动素化学全合成。

促肠活动素的仿生全合成
第二个例子,则是抗疟一线药物:青蒿素。这是一种含有少见的过氧桥的倍半萜内酯类化合物,自 1970 年代中国科学家从青蒿中发现该分子以来,以青蒿素及其衍生物为基础的青蒿素联合疗法,已经成为现今全球范围内治疗恶性疟原虫疟疾的标准方法。
为了提供稳定的来源,来自加州大学伯克利分校的 Jay D. Keasling 团队发了一个细胞工厂,将青蒿素生物合成途径相关的基因导入到了酿酒酵母当中,最终成功实现了青蒿素前体青蒿酸的生产,浓度为 100 mg/L。
在此基础之上,来自 Amyris 等研究人员采用了多种合成生物学策略,包括了启动子工程、密码子优化以及功能基因替换,来用以增强酵母生产青蒿酸的能力,最终,他们将浓度提高到相当高的 25 g/L。
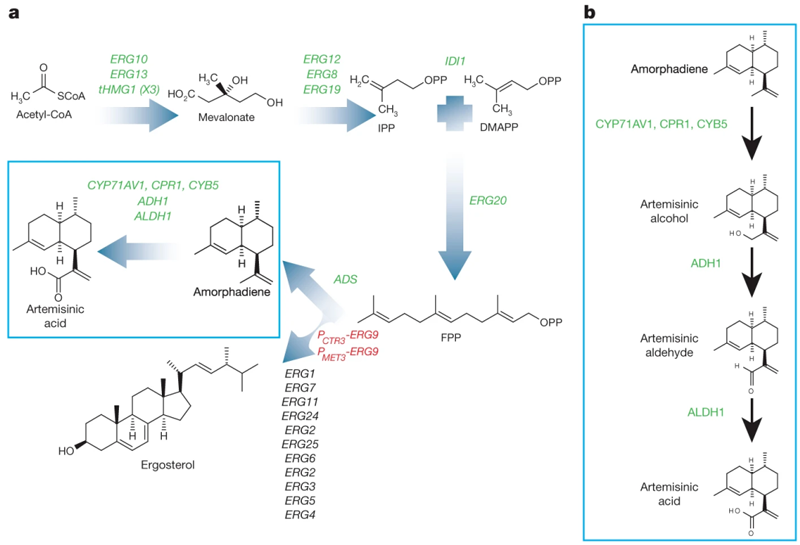
酵母中的青蒿酸生产途径(来源:Nature)
这一成就使得他们能够建立一个可扩展的合成路线,下游衔接激发态氧分子的化学方法,将青蒿酸进一步转化成为青蒿素。这项成果是合成生物学领域当中的典型案例,其代表了合成生物学和化学协同的新领域,以解决自然界中有限的高附加值产品的生产和供应问题。
不难看出,在上述两个例子当中,利用合成生物学进行设计与合成的对象,都是天然产物。而在这第三个例子则与之所有所不同,其是关于非天然类似物的。
通常来说,酶具有严格的底物特异性,因此,开发非自然复杂分子的全酶合成一直是一个挑战。不过,随着技术的进步,现在这一延伸目标已经触手可及。这其中的典型示例,便是用于合成核苷类似物依拉曲韦(Islatravir)的多酶级联反应,这是默克公司正在研究的一种抗 HIV 药物。
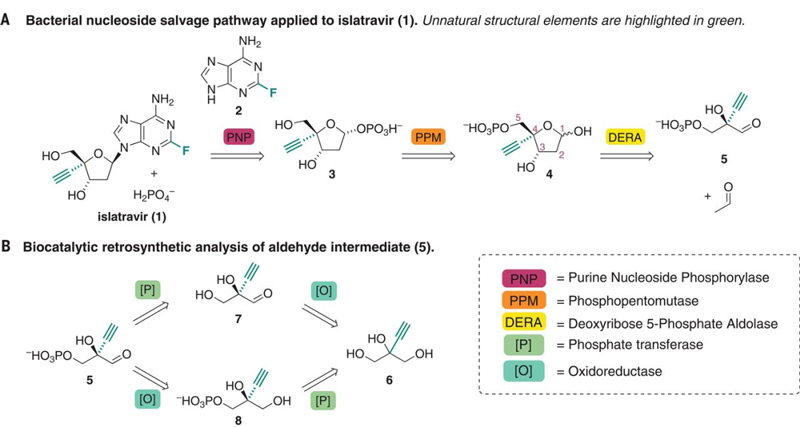
核苷补救合成途径的逆向设计(来源:Science)
该级联反应基于细菌核苷补救合成途径的逆向设计,之后,研究人员通过定向进化设计并优化了 5 种酶,使其能够作用于非天然底物并在反应条件下保持稳定。最终,这些酶与四种辅助酶一起,实现了在 3 步生物催化级联中立体选择性地组装依拉曲韦。
该项研究达到了 51% 的总产率,由于该工艺去除了中间纯化和保护,因此其与之前报道的化学合成工艺相比(12 步,总产率 15%),生产步骤更少且产率更高。这是一项杰出的工作,其展示了一种利用生物合成酶合成复杂非天然分子的不同策略。
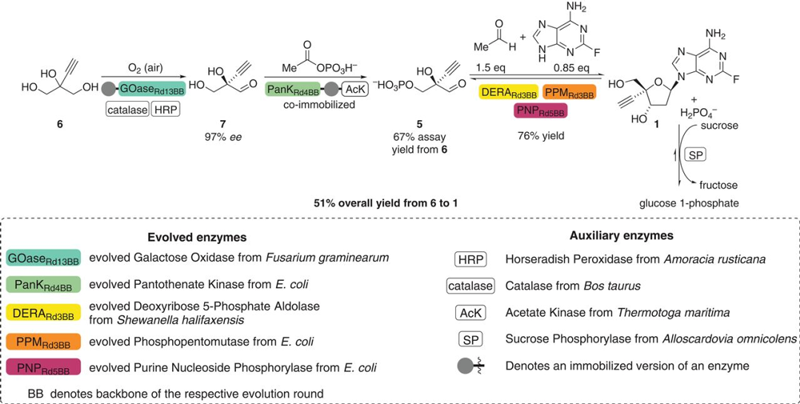
用于生产依拉曲韦的体外生物催化级联设计(来源:Science)
“正如前文所述,随着合成生物学的出现,我们可能正在进入小分子全合成的新时代。具体而言,合成生物学在小分子合成中提供了高效率、无与伦比的精度和不可或缺的可持续性,而化学方法则提供了更大的可变性和多样性。”
因此,小分子合成的未来,无疑将是由化学和生物学的结合推动。鉴于这两个领域的复杂性,合成化学家或生物学家可能很难单独进行推动。因此在最后,研究人员呼吁道:“迫切需要通过社群的努力,来改变全合成领域。”
原文信息:
Harnessing nature's biosynthetic capacity to facilitate total synthesis
文章来源 | 解码合成生物
编辑 | 鲍 啦
欢迎投稿、建议 | media@szbl.ac.cn