2022年12月8日,深圳湾实验室生物医学工程研究所郭腾飞课题组在国际阿尔茨海默病协会官方杂志Alzheimer's & Dementia 上发表题为“Presynaptic membrane protein dysfunction occurs prior to neurodegeneration and predicts faster cognitive decline”的文章,阐述了CSF GAP-43与神经退行性变的关系及这两者对认知能力下降的影响,证实了突触前膜蛋白功能障碍的发生早于神经退行性改变并且预示更快的认知下降。
阿尔茨海默病(Alzheimer’s disease, AD)是老年人中最常见慢性神经退行性疾病,也是造成痴呆的主要病因,其主要病理特征为β-淀粉样蛋白(β-amyloid, Aβ)和tau蛋白异常聚集形成的淀粉样蛋白斑块和神经原纤维缠结。在包括AD在内的各种神经退行性疾病中,进行性突触功能障碍是与神经元死亡密切相关的基础病理变化。既往研究发现可溶性Aβ及磷酸化tau均可引起突触损伤,并且对突触前膜的损伤较突触后膜明显。
生长相关蛋白-43(growth-associated protein-43, GAP-43)是一种主要表达于海马和相关皮层的突触前膜蛋白,负责调控大脑轴突生长、突触发生和突触可塑性等过程。已有研究在AD患者中观察到脑脊液(cerebrospinal fluid, CSF) GAP-43水平升高,反映了突触前的功能障碍。尽管目前认为CSF GAP-43与AD显著相关,但CSF GAP-43与神经退行性变间的顺序关联仍未研究清楚。
2022年12月8日,深圳湾实验室生物医学工程研究所郭腾飞课题组在国际阿尔茨海默病协会官方杂志Alzheimer's & Dementia 上发表题为“Presynaptic membrane protein dysfunction occurs prior to neurodegeneration and predicts faster cognitive decline”的文章,阐述了CSF GAP-43与神经退行性变的关系及这两者对认知能力下降的影响,证实了突触前膜蛋白功能障碍的发生早于神经退行性改变并且预示更快的认知下降。
研究纳入了国际知名AD纵向研究队列(Alzheimer's Disease Neuroimaging Initiative,ADNI)中的730名受试者,均有基线Aβ 及FDG PET、CSF p-Tau181、CSF GAP-43以及纵向核磁共振(MRI)和认知评估数据,其中327名受试者同时有纵向Aβ PET、CSF p-Tau181、CSF GAP-43数据。首先,该研究根据Aβ PET、CSF p-Tau181、剩余海马体积(residual hippocampal volume, rHCV)或葡萄糖代谢情况(MetaROIs FDG SUVR)将参与者分为不同的生物学阶段(A/T/N),并比较了基线和纵向CSF GAP-43在AD不同生物学阶段的变化情况。研究发现,无论是使用rHCV还是MetaROIs FDG SUVR定义神经退行性变,A-/T+/N-, A-/T+/N+, A+/T+/N-, A+/T+/N+组均具有更高的CSF GAP-43蛋白浓度以及更快的增加速率(图1)。这说明脑中异常的tau病理是影响CSF GAP-43的关键因素。
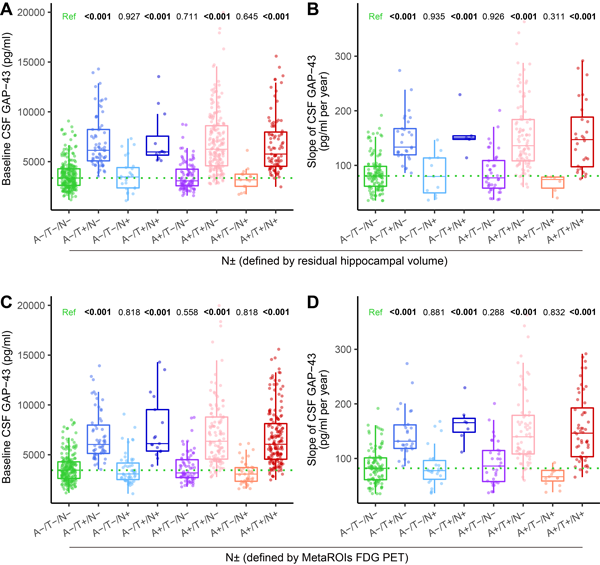
图1. CSF GAP-43在AD不同阶段的横断面和纵向比较。A:Aβ PET、T: CSF p-Tau181、N: 海马体积(residual hippocampal volume, rHCV)或葡萄糖代谢(MetaROIs FDG SUVR)
该研究进一步分析了CSF GAP-43与海马、皮质萎缩和代谢减低的关系。作者发现,基线CSF GAP-43浓度可以预测未来更快的海马体积萎缩、皮层厚度变薄和糖代谢缺失(图2A-C)。相反的是,基线的海马体积、皮层厚度及糖代谢水平并不能预测纵向的CSF GAP-43浓度变化(图 2D-F)。以上结果提示,CSF GAP-43异常升高可能比FDG PET或结构MRI检测到的神经退行性变更早发生。
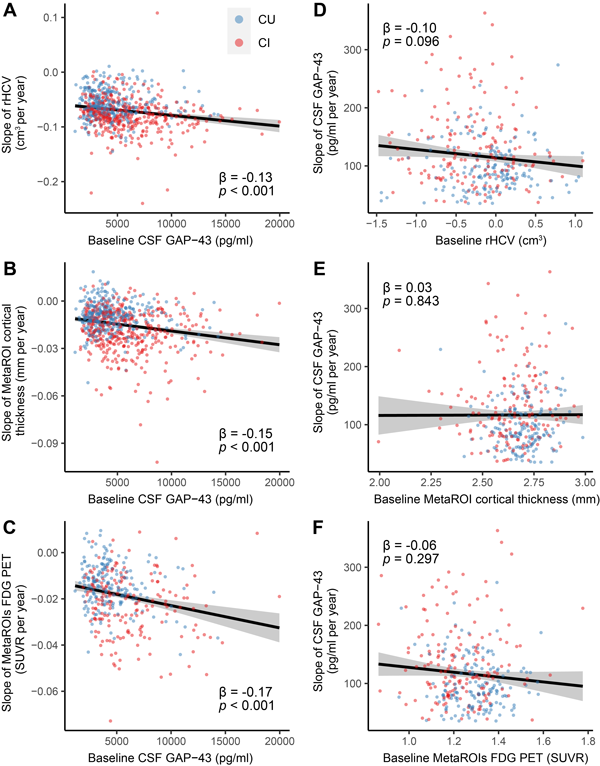
图2. CSF GAP-43与海马萎缩、AD典型皮层区域MetaROIs皮质变薄和糖代谢缺失的关系
为了验证这一假说,作者进一步探索了CSF GAP-43与68个不同脑区灰质体积及皮层厚度的关系,发现基线CSF GAP-43浓度与28个脑区的灰质体积萎缩速率及40个脑区的皮层厚度减低率呈负相关(图 3A, B)。其中,相关性最强的脑区是颞中部(图3C, D)。相反,基线颞中部灰质体积和皮质厚度同样无法预测纵向的CSF GAP-43浓度变化(图3E-F)。进一步证实上述假说,即CSF GAP-43异常升高要早于神经退行性变的发生。
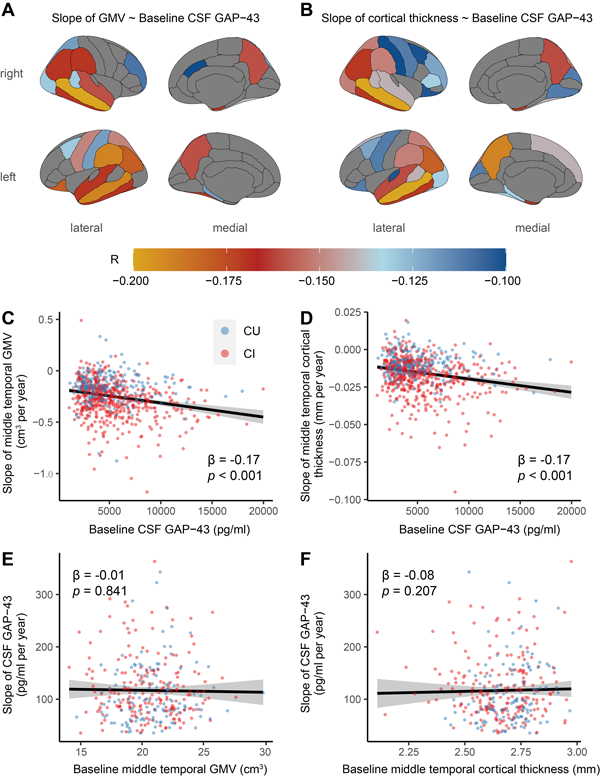
图3. CSF GAP-43与不同区域灰质体积及皮层厚度的相关性
最后,考虑到突触功能障碍是AD早期的病理改变之一,与认知功能损伤密切相关,该研究分析了CSF GAP-43与神经退行性变在认知能力下降中的相互作用。作者发现,基线CSF GAP-43与metaROIs FDG SUVR及颞中部灰质体积在预测纵向认知衰退方面存在显著相互作用(图4),较高的基线CSF GAP-43浓度提示更快的认知下降速率。这说明突触前的功能障碍可能早于脑萎缩、代谢减低等神经退行性变发生,并且与认知下降存在密切关系。
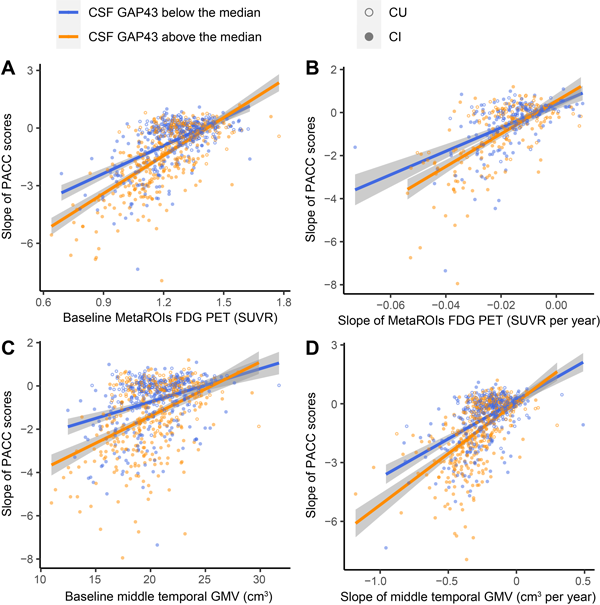
图4. CSF GAP-43与神经退行性变在认知能力下降中的相互作用
综上所述,该研究揭示了CSF GAP-43在AD不同生物学阶段的变化情况,并探究了其与神经退行性变及认知下降的关系。本研究提示脑内异常tau病理可能是导致突触前损伤的关键,这种损伤先于神经退行性变的发生,并提示较快的认知下降。这为进一步理解AD病理、突触前损伤、神经退行性变、认知下降间的复杂关系提供了新思路,并提示我们早期针对tau病理的治疗可能有助于减少突触功能障碍进而减缓脑结构损伤及认知下降。
郭腾飞研究员为论文通讯作者。深圳湾实验室生物医学工程研究所博士后兰国钰为论文第一作者。郭腾飞课题组副研究员刘振,香港科技大学联培博士生李安琪以及清华国际研究生院马少华教授为本论文合作者。该研究获得国家自然科学基金面上项目(82171197)、深圳湾实验室重大项目培育项目(S211101002-2)和开放基金项目(SZBL2020090501014)联合资助。
郭腾飞课题组(http://guotf-lab.szbl.ac.cn/)主要致力于研究阿尔茨海默病(Alzheimer’s disease, AD)的病理特征及演化规律,开发AD早期的诊疗新技术。近五年来,以第一作者/通讯作者在AD领域顶级期刊Alzheimer’s & Dementia (2018, 2022)、Biological Psychiatry (2021)、Annals of Neurology (2022)、Neurology (2020a, 2020b)、Journal of Nuclear Medicine (2017)、Alzheimer’s Research & Therapy (2020, 2021)、Translational Psychiatry(2022)等杂志发表多篇原创学术文章,对于理解AD的病理特征、发病机制、演化规律以及临床试验具有重要的科学意义和临床价值。目前团队获得国家自然科学基金面上项目、广东省杰出青年基金等项目支持。课题组的主要研究兴趣包括:1)使用多模态神经影像(PET和MRI)和生物标记物 (CSF 和plasma Aβ42, Aβ40 and p-Tau) 开展AD早期诊断研究;2)借助于AD类器官或者动物模型进一步验证和拓展AD相关的临床研究发现;3)开发AD早期干预新技术(超声神经刺激等)和透明病理成像新技术。团队借助于生物标记物、生物化学方法、多模态神经影像技术、超声神经刺激技术探究AD早期诊断和干预治疗方案,正在联合深圳湾实验室其他课题组以及国内多家知名临床医院深入研究和解析AD临床前阶段的病理特征、风险因素、保护指标和演化规律,为我国AD临床前阶段的早期诊断和干预治疗提供科学依据。此外,课题组将结合AD类器官模型、AD动物模型、微流控及动物成像开展AD发病机理研究。真诚邀请欢迎有志于大脑神经退行性疾病早期诊疗的科研工作者(助理研究员/博士后/博士研究生)加入我们的课题组。
原文信息:
文章来源 | 郭腾飞课题组
编辑 | 鲍 啦
欢迎投稿、建议 | media@szbl.ac.cn