Everyone shines in their own way.
王晖
Hui WANG
粤港澳生物医学创新中心
特聘研究员
hwang@szbl.ac.cn
Timeline
-
2021 至今
深圳湾实验室 特聘研究员
-
2015-2021
霍华德休斯医学研究所华盛顿大学 研究专员
-
2009-2015
霍华德休斯医学研究所华盛顿大学 博士后
-
2008-2009
南开大学 研究助理
-
2002-2008
清华大学 博士
-
1998-2002
四川大学 学士
研究领域
以铁生物学为主线,关注铁代谢、铁稳态、铁死亡等由铁参与调控的重要生物学过程,本课题组的研究方向包括但不限于:
1)铁代谢中的蛋白质稳态调控
2)铁介导的氧化还原水平感知 (redox sensing)
3)全新含铁蛋白的发现和功能鉴定
4)借由铁水平感知实现靶向蛋白质降解 (TPD)
5)设计小分子干预铁代谢/铁稳态,诱导肿瘤细胞铁死亡
成果
王晖博士毕业于清华大学医学院,师从饶子和院士;随后在霍华德休斯医学研究所 (HHMI) 华盛顿大学郑宁教授实验室进行博士后工作,并留任研究所,其间主要从事铁代谢过程中的蛋白质稳态研究。她首次发现了铁硫簇可以作为关键的氧化还原开关 (redox switch) 存在于真核细胞泛素化系统中,通过改变自身氧化还原状态感知氧气和氧化还原水平的变化,实现对细胞铁稳态的调控。该研究不仅揭示了一个全新的铁稳态调节机制,而且确立了铁硫蛋白在细胞氧气及氧化还原水平感知过程中的重要作用。此外,王晖博士还从事了多项RNA代谢/稳态调控方面的研究,并以第一作者身份在Molecular Cell、Nature Structural & Molecular Biology、Cell Research、The EMBO Journal、Journal of Molecular Biology等期刊上发表多篇文章,其成果被Molecular Cell、Nature Chemical Biology、Science Signaling、The EMBO Journal、F1000、BioArt等专文点评或推荐。
代表性图片
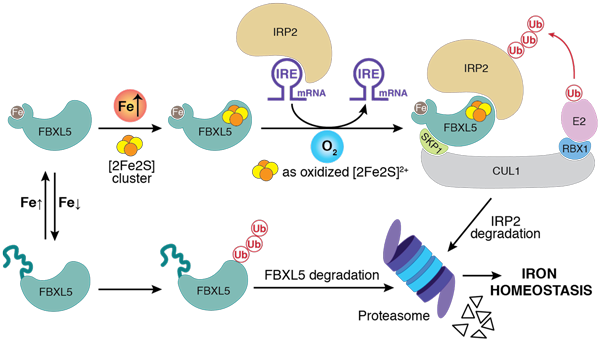
Mol Cell. 2020, 78(1): 31-41
王晖博士发现泛素酶FBXL5通过自身铁硫簇辅因子感知细胞内氧气水平调控铁稳态
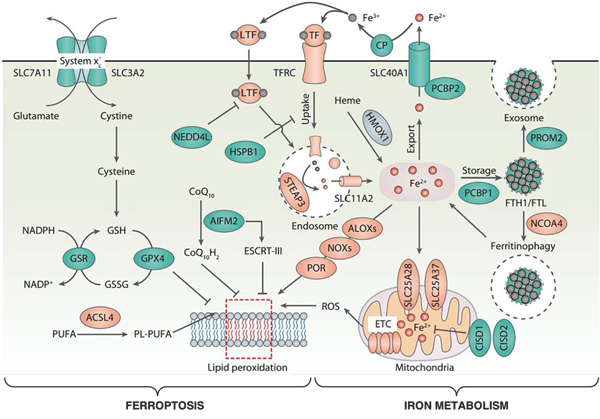
Front Cell Dev Biol. 2020, Oct 7;8:590226.
本课题组将长期致力于铁代谢对于铁死亡的调控和影响的机制研究
荣誉奖励
• 2019 HHMI工作贡献奖
• 2005 清华大学通用电气奖学金
• 2004 清华大学光华奖学金
• 2002 四川大学优秀毕业生干部
• 2002 四川大学迪康奖学金
招聘信息
1. 助理研究员
2. 博士后
新闻报道
Preview, Mol Cell. 2020, 78(1): 1-3, https://doi.org/10.1016/j.molcel.2020.03.020
Research Highlight, Nat Chem Biol. 2020, 16(5): 481, https://doi.org/10.1038/s41589-020-0536-7
Editors’ Choice, Sci Signal. 2019, 12(588): eaay5593, https://doi.org/10.1126/scisignal.aay5593
News & Views, EMBO J. 2020, 39(8): e104744, https://doi.org/10.15252/embj.2020104744
代表论文
1. Wang H*, Shi H*, Rajan M, Canarie RE, Hong S, Simoneschi D, Pagano M, Bush FM, Stoll S, Leibold AE, Zheng N. FBXL5 regulates IRP2 stability in iron homeostasis via an oxygen-responsive [2Fe2S] cluster. Mol Cell. 2020, 78(1): 31-41.
2. Kuchay S*, Wang H*, Marzio A, Jain K, Homer H, Fehrenbacher N, Philips MR, Zheng N, Pagano M. GGTase3 is a newly identified geranylgeranyltransferase targeting a ubiquitin ligase. Nat Struct Mol Biol. 2019, 26(7): 628-636.
3. Wang H, Curran EC, Hinds TR, Wang EH, Zheng N. Crystal structure of a TAF1-TAF7 complex in human transcription factor IID reveals a promoter binding module. Cell Res. 2014, 24(12): 1433-1444.
4. Wang H, Morita M, Yang X, Suzuki T, Yang W, Wang J, Ito K, Wang Q, Zhao C, Bartlam M, Yamamoto T, Rao Z. Crystal structure of the human CNOT6L nuclease domain reveals strict poly(A) substrate specificity. EMBO J. 2010, 29(15): 2566-2576.
5. Wang H*, Pang H*, Bartlam M, Rao Z. Crystal structure of human E1 enzyme and its complex with a substrate analog reveals the mechanism of its phosphatase/enolase activity. J Mol Biol. 2005, 348(4): 917-926.