过往不恋,未来不迎,当下不杂
李芬芳
Fenfang LI
生物医学工程研究所
Timeline
-
2022 至今
深圳湾实验室 特聘研究员
-
2019-2021
李光前医学院 (伦敦帝国学院与南洋理工大学联合办学) 院长研究基金博士后
-
2015-2019
杜克大学 博士后
-
2010-2015
新加坡南洋理工大学 物理与应用物理系 博士
-
2006-2010
武汉大学 材料物理学士
研究领域
研究领域主要包括生物医学超声空化的流体力学、生物学效应和力学信号转导,微流控中单细胞力学性能分析,探索相关机理并开发超声力学调控技术用于肿瘤和神经系统,以及微流控器件早期检测癌细胞入侵性和药物筛选。
成果
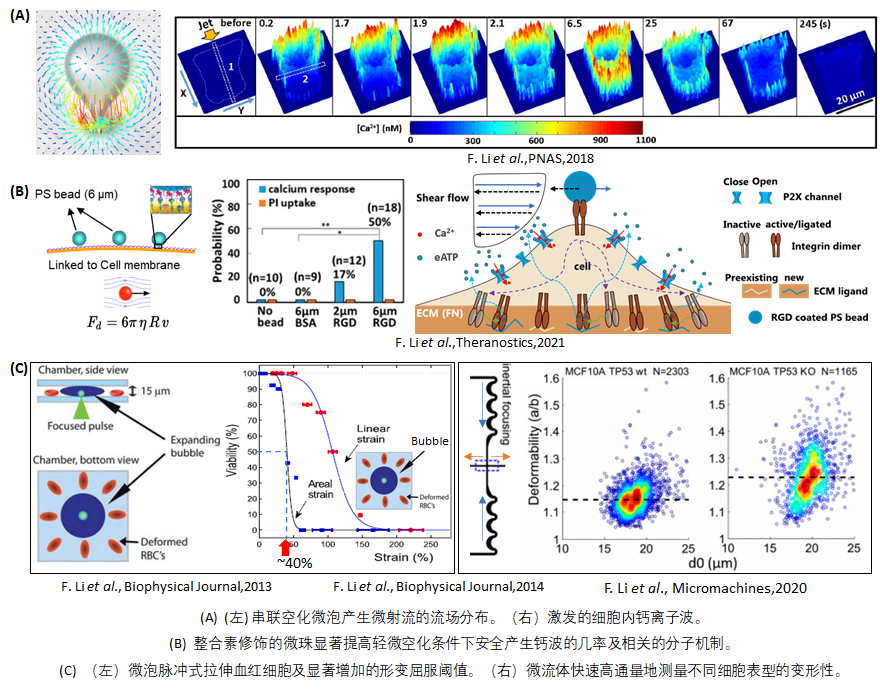
空化是治疗超声的重要机制,但难以控制和明确其物理和生物效应。李芬芳博士围绕空化微泡在细胞及分子水平的流体力学效应和生物效应等关键问题开展系统研究。取得的主要创新性成绩包括:
(1)从生物物理学角度揭示了高强度空化力学拉伸和破坏细胞的机制;
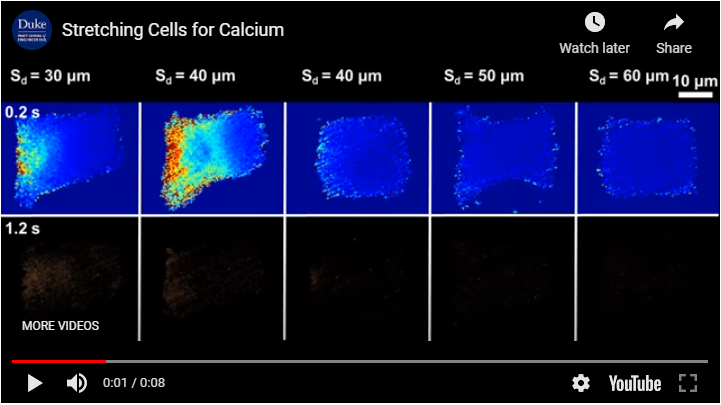
(2)实现了高度可控的空化与细胞的相互作用,揭示了中低强度空化使细胞产生钙波反应的两种不同机制分别与细胞膜破孔和力感离子通道被激活有关;
(3)提出了使轻微空化安全有效激发细胞内钙信号的新策略,并揭示了其关键的力学敏感分子机制。
此外,还利用单细胞流体动力学拉伸或微筛等瞬时快速的微流体实现了高通量无标记地测量癌细胞的机械特性并与其表型和遗传学联系。
该系列研究为声穿孔药物控释、超声神经调控、癌细胞入侵性进展的早期检测等前沿应用提供了科学理解和新思路。
研究成果发表在PNAS, Theranostics,Biophysical Journal, Physical Review Fluid 等领域内一流期刊。研究工作被Nature, PNAS,Theranostics, Advanced Science, Journal of Controlled Release 等国际一流杂志正面引用,并被The Medical News, EurekAlert, Scitech Daily, Phys.org等知名学术网站报道。受邀担任空化领域重要国际学术会议的分会主席一次。获得过李光前医学院院长研究基金的声学基因控制项目(39万新加坡币,约195万人民币,英国伦敦帝国学院和新加坡南洋理工大学的联合项目, 每年只有一个名额)。
荣誉
• 2019-2021 李光前医学院院长博士后研究基金
• 2012 微流体生物医学应用会议最佳海报奖
• 2010-2014南洋理工大学博士研究奖学金
招聘信息
媒体报道
1. A Safer Route to Ultrasonic Therapy(Microbeads allow ultrasonic waves to stimulate cells more safely):
https://pratt.duke.edu/about/news/calcium-cavitation
https://www.eurekalert.org/news-releases/690167
2. Researchers discover way to enhance effectiveness and safety of sonogenetics
3. Duke University Enhances the Effectiveness and Safety of Sonogenetics
4. Microbeads allow ultrasonic waves to stimulate cells more safely
代表论文
(1) Fenfang Li; Chen Yang; Fang Yuan; Defei Liao; Thomas Li; Farshid Guilak; Pei Zhong*; Dynamics and mechanisms of intracellular calcium waves elicited by tandem bubble induced jetting flow, Proceedings of the National Academy of Sciences , 2018, 115(3): E353-E362.
(2) Fenfang Li*; Tae Hyun Park; George Sankin; Christopher Cilchrist; Defei Liao; Chon U Chan; Zheng Mao; Brenton D. Hoffman*; Pei Zhong*; Mechanically induced integrin ligation mediates intracellular calcium signaling with single pulsating cavitation bubbles, Theranostics, 2021, 11(12): 6090-6104.
(3) Fenfang Li*; Igor Cima; Jess Honganh Vo; Min-Han Tan; Claus Dieter Ohl*; Single cell hydrodynamic stretching and microsieve filtration reveal genetic, phenotypic and treatment-related links to cellular deformability, Micromachines, 2020, 11(5): 486.
(4) Defei Liao, Fenfang Li, David Lu, Pei Zhong*; Activation of Piezo1 mechanosensitive ion channel in HEK293T cells by 30 MHz vertically deployed surface acoustic waves, Biochemical and biophysical research communications 2019, 518 (3), 541-547
(5) Fenfang Li, Chon U Chan, Claus Dieter Ohl*; Yield strength of human erythrocyte membranes to impulsive stretching, Biophysical journal, 2013, 105 (4), 872-879