
2026年3月31日,深圳湾实验室彭琴课题组、重庆大学邱菊辉课题组与华南理工大学李趣欢等合作在EMBO Reports上在线发表了题为 Matrix Stiffness Induces Midnolin-dependent Lamin B1 Degradation to Control Myoblast Differentiation 的最新研究成果。该研究发现,软基质力学微环境中,成肌细胞里的核纤层蛋白Lamin B1水平显著下降,分化能力严重受阻。主要分子机制是软基质刚度启动了Midnolin与Lamin B1互作,通过非泛素依赖的蛋白酶体降解途径显著下调Lamin B1水平,来响应外界不适的力学微环境。阻断Midnolin-Lamin B1通路可挽救软基底引起的成肌分化缺陷。因此,维持适度的Lamin B1水平才能保证成肌细胞的正常分化。换句话说,成肌细胞的分化如同在不同硬度的基石上构建大厦,Lamin B1则是支撑核心的‘动态支架’。只有根据分化阶段精准调节支架的强度,细胞才能顶住环境压力,最终发育成形态稳固、功能完备的成熟建筑。

力学微环境,如细胞外基质(ECM)刚度与机械载荷,是调控干细胞及前体细胞功能与命运决定的关键因素[1]。细胞通过感知这些机械信号并激活下游信号通路,最终实现细胞命运调控[2]。特别是在骨骼肌系统中,ECM的结构重构与刚度变化与杜氏肌营养不良等病理过程密切相关。研究证实,机械负荷的降低或基底刚度的减弱会显著抑制成肌细胞的分化程序与肌肉组织的修复再生,这是导致废用性肌肉萎缩的关键诱因[3]。作为细胞内物理性质最坚硬的细胞器,细胞核是感知并响应力学信号的核心枢纽。它通过细胞骨架与核骨架连接(LINC)复合物,将胞外物理信号转化为胞内生物化学反应[4, 5]。这种机械感知能力使细胞核能够动态调节其形态与功能,其对机械力信号的动态调整被称为“核力学适应(Nuclear mechano-adaptation)”,其核心在于核骨架蛋白的迅速重构以维持核结构的完整性[4]。在维持核稳态的各类蛋白中,核纤层蛋白(Lamina protein)发挥着关键支架作用。其中,Lamin B1对调节核弹性及稳定染色质状态至关重要[6]。然而,关于Lamin B1如何实时响应力学微环境变化的动力学规律及其分子机制,仍不清楚。
研究团队利用聚丙烯酰胺水凝胶构建了两种不同刚度的生长环境:0.2 kPa(模拟萎缩肌肉的软基底)和10 kPa(模拟健康肌肉的硬基底)。转录组测序分析显示,在软基底环境下,与细胞命运决定、细胞分化及DNA修复相关的信号通路均发生了显著下调。实验结果进一步证实,在软基底上诱导分化时,原代成肌细胞与C2C12成肌细胞系的融合能力均受到严重抑制。进一步探究发现,这种抑制作用源于一系列时间相关的细胞力学适应(Mechanoadaptation)过程:在接触软基底的数分钟内,成肌细胞的早期铺展能力受限,F-actin组装受阻,导致细胞核体积显著缩小。随后在24小时内,出现了明显的核形态异常,包括核出泡(blebbing)和微核(MN)的形成。值得注意的是,这种核形态的异常早于DNA损伤的显著积累。随着培养时间的增加,软基底上的细胞表现出更高水平的gH2AX(DNA损伤标志物)阳性信号(图1)。
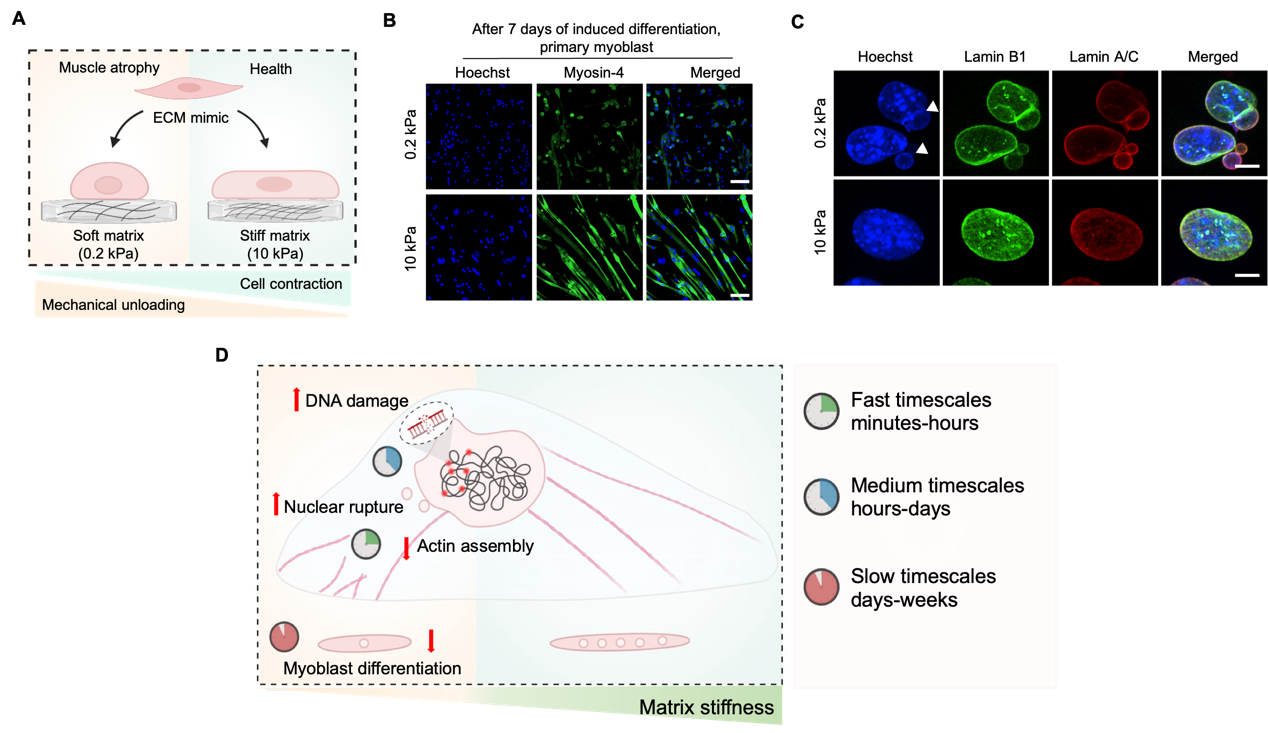
图1 软基底诱导成肌分化障碍及细胞核异常
研究团队通过对多种机械转导通路相关的核膜蛋白进行系统筛选发现,在模拟肌肉萎缩的软基底(0.2 kPa)环境下,核纤层蛋白 Lamin B1 的水平在细胞感知机械信号短时间内(Minutes)即发生最为显著的下调,且该响应在原代成肌细胞及多种细胞系中均具有高度保守性。为了解析这一现象的动力学过程,转录组测序与蛋白质合成抑制实验证实,软基底诱导的Lamin B1 减少并非源于mRNA 转录抑制或蛋白质翻译受损,而是由蛋白酶体途径介导的蛋白质降解加速所驱动。进一步机制研究表明,该降解过程并不依赖传统的泛素化修饰,而是涉及一种由核蛋白Midnolin介导的新的非泛素依赖性降解途径[7]。实验证实,Midnolin在软基底环境下能特异性识别并结合 Lamin B1,敲低Midnolin可显著恢复软基底环境下的Lamin B1 水平。结合 AlphaFold 结构预测与实验分析,Midnolin包含一个名为“Catch”的特定结构域[7],能够直接识别并捕获 Lamin B1 的 Ig 样结构域。这种直接的蛋白互作将Lamin B1递送至蛋白酶体进行降解,且该过程受基底硬度精确调控(图2)。
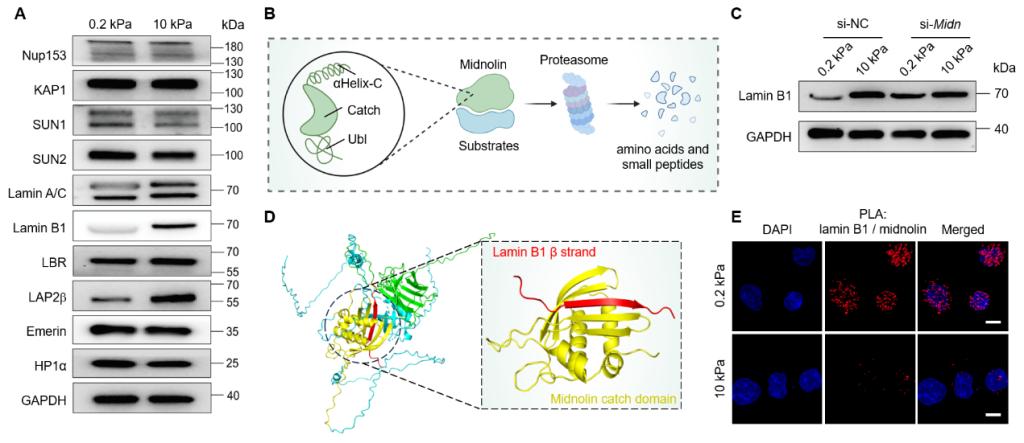
图2 软基底诱导Midnolin直接结合Lamin B1并介导其降解
研究团队进一步探究了 Midnolin 介导的 Lamin B1 降解在成肌分化中的功能意义。实验结果显示,在软基底环境下,通过敲低 Midnolin的水平或表达无法与 Midnolin 结合的 Lamin B1 突变体(缺失midnolin结合位点),能够有效阻断Lamin B1的异常降解并显著挽救成肌分化缺陷。Lamin B1的完全缺失或水平降低会导致成肌分化程序受抑制,证明其为分化启动的必要因子。进一步分析揭示,Lamin B1在分化诱导后的早期阶段(hours)呈现瞬时高表达,这一窗口期对于激活下游信号至关重要。机制研究发现,Lamin B1 能够精准调控非经典Wnt信号通路关键因子Wnt4以及肌原性调节因子Myod1 的表达,从而调控成肌分化。此外,Lamin B1 的下调还导致了显著的gH2AX阳性信号累积,表明其在分化过程中对维持基因组稳定性不可或缺(图3)。
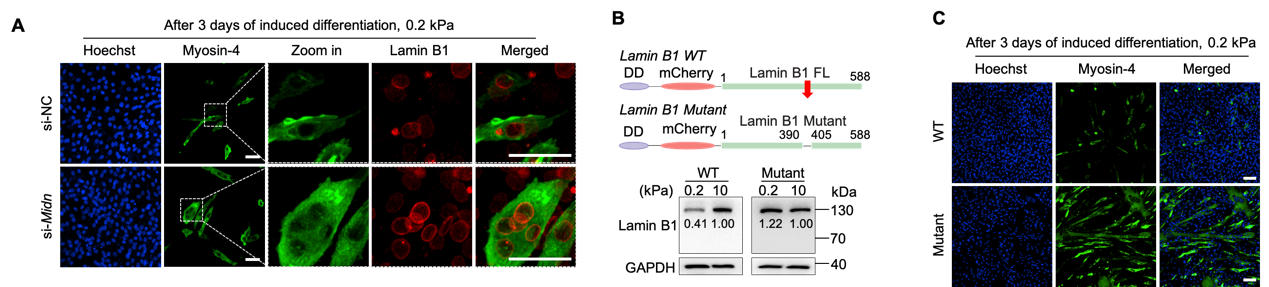
图3 阻断Midnolin-Lamin B1通路可挽救软基底引起的成肌分化缺陷
综上所述,该研究发现了一种新型的、不依赖泛素化的核机械响应机制:在机械信号的刺激下,midnolin会介导Lamin B1的蛋白酶体降解,从而导致核结构完整性丧失,最终决定肌原性调节因子相关基因的表达。这一工作不仅深化了对细胞机械信号转导机制的理解,也为开发针对肌肉萎缩等疾病的治疗策略提供了潜在的新靶点。
深圳湾实验室系统与物理生物学研究所特聘研究员彭琴、重庆大学邱菊辉研究员及华南理工大学李趣欢副教授为本文通讯作者。深圳湾实验室-哈尔滨工业大学联合培养博士生郭利苹、深圳湾实验室-香港科技大学联合培养博士生赵彦菁等为本文共同第一作者。感谢深圳湾实验室系统与物理生物学研究所资深研究员周耀旗、深圳湾实验室分子生理学研究所特聘研究员张洋、香港科技大学阎言教授、深圳湾实验室系统与物理生物学研究所助理研究员张哲博士等为本研究做出了重要贡献。该研究得到了国家自然科学基金、深圳市医学研究专项资金项目、深圳湾实验室大型仪器开放共享基金等的资助。
参考文献
1. De Belly, H., E.K. Paluch, and K.J. Chalut, Interplay between mechanics and signalling in regulating cell fate. Nat Rev Mol Cell Biol, 2022. 23(7): p. 465-480.
2. Engler, A.J., et al., Matrix elasticity directs stem cell lineage specification. Cell, 2006. 126(4): p. 677-89.
3. Kjaer, M., Role of extracellular matrix in adaptation of tendon and skeletal muscle to mechanical loading. Physiol Rev, 2004. 84(2): p. 649-698.
4. Kalukula, Y., et al., Mechanics and functional consequences of nuclear deformations. Nat Rev Mol Cell Biol, 2022. 23(9): p. 583-602.
5. Dupont, S. and S.A. Wickstrom, Mechanical regulation of chromatin and transcription. Nat Rev Genet, 2022. 23(10): p. 624-643.
6. Wintner, O., et al., A Unified Linear Viscoelastic Model of the Cell Nucleus Defines the Mechanical Contributions of Lamins and Chromatin. Adv Sci (Weinh), 2020. 7(8): p. 1901222.
7. Gu, X., et al., The midnolin-proteasome pathway catches proteins for ubiquitination-independent degradation. Science 2023. 381(6660): p. eadh5021.
原文信息:
Matrix Stiffness Induces Midnolin-dependent Lamin B1 Degradation to Control Myoblast Differentiation

 粤公网安备44031102000926号
粤公网安备44031102000926号