
电话:+86-755-86967710
邮箱:webmaster@szbl.ac.cn

分子生理学研究所
mikexzhu(at)szbl.ac.cn
细胞内钙信号传导,离子通道(包括细胞器离子通道),膜受体,G蛋白偶联受体(GPCR)与G蛋白信号转导,自噬,细胞死亡机制,细胞内囊泡运输,溶酶体,细胞内水跨膜转运,神经退行性病变,自闭症,中风,疼痛,瘙痒,炎症,纤维化,糖尿病,脂肪性肝病,皮肤病,癌症
资深研究员
正教授
助理教授/副教授
助理研究员
博士后
博士后
博士 (PhD)
硕士 (M.S.)
学士 (B.S.)
离子稳态和离子通道的分子与细胞调控机制及其失调导致疾病的原理。主要研究领域包括钙信号传导、瞬时受体电位(TRP)通道、酸敏感离子通道(ASICs)以及内溶酶体双孔通道(TPCs)。我们利用细胞和动物模型研究其在神经发育、神经传递、疼痛/瘙痒以及神经退行性病变中的作用。同时,我们还探索这些通道在心脏、肺、肝、肠道、皮肤和免疫细胞等其他器官中的功能及致病机理。
钙离子对细胞功能至关重要,钙信号一直是生物医学研究的重要领域之一。朱曦博士的研究专注于细胞钙信号、离子通道、膜受体和G蛋白信号转导,重点集中于细胞信号传导和离子通道调控分子机制和生理病理功能,主要成果包括:
·基因克隆并功能表达哺乳动物经典瞬时受体电位(TRPC)通道以及后续对多类TRP通道功能调控与生理病理作用的深入研究。
·基因克隆双孔通道(TPC)并验证其响应NAADP诱发溶酶体钙离子释放的功能,后续研究进一步证明TPC同时响应磷脂酰肌醇PI(3,5)P2并在多个细胞生理过程和疾病中发挥重要作用。
·发现酸敏感通道亚型1a (ASIC1a)通过非通道功能激活RIPK1导致细胞酸中毒并阐明其分子作用机理,应用场景包括脑卒中和多种神经退行性疾病。
朱曦博士的学术影响力、专业知识及学术贡献受到国际同行的广泛认可,曾参与TRP通道正名全过程,数次受邀参加戈登研究会议(GRC)和FASEB SRC等国际顶级会议及论坛,并作报告;在Cell,Nature和Nature子刊等权威期刊发表相关文章两百多篇。
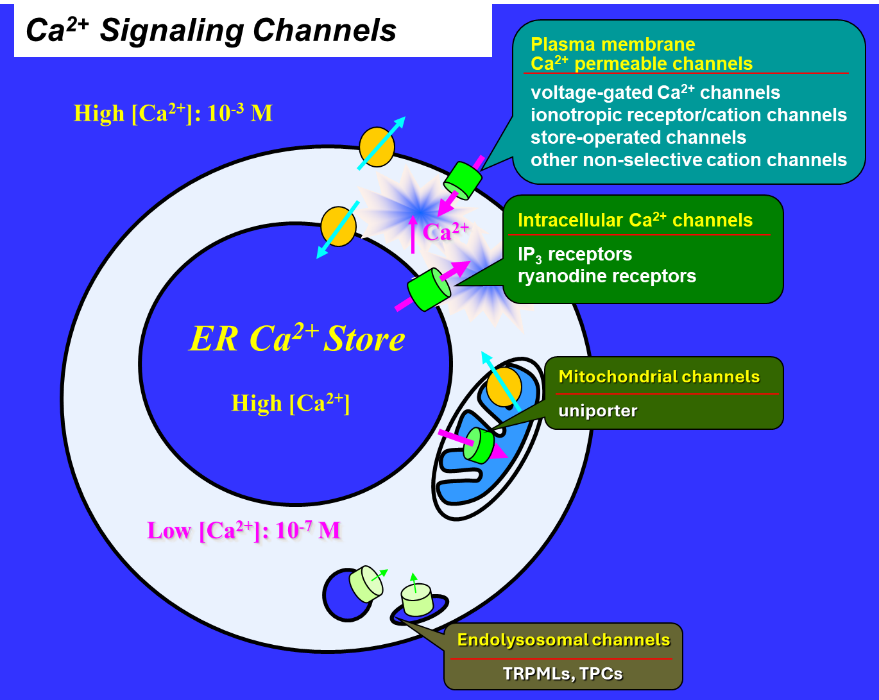
图1.钙信号传导原理。在静息状态下,细胞维持极低的胞质钙离子浓度([Ca2+],约100 nM)。细胞外空间以及内质网(ER)和内体/溶酶体(统称为内溶酶体)腔内的钙离子浓度则处于毫摩尔水平。当质膜、内质网膜及内溶酶体膜上的钙离子通透性通道开放时,钙离子流入胞质,导致胞质[Ca2+]升高。钙信号在细胞的存活与死亡过程中发挥着至关重要的作用。此外,钙离子还可进入线粒体以调节其功能。图中标识了不同细胞区室中的主要钙离子通道类型。
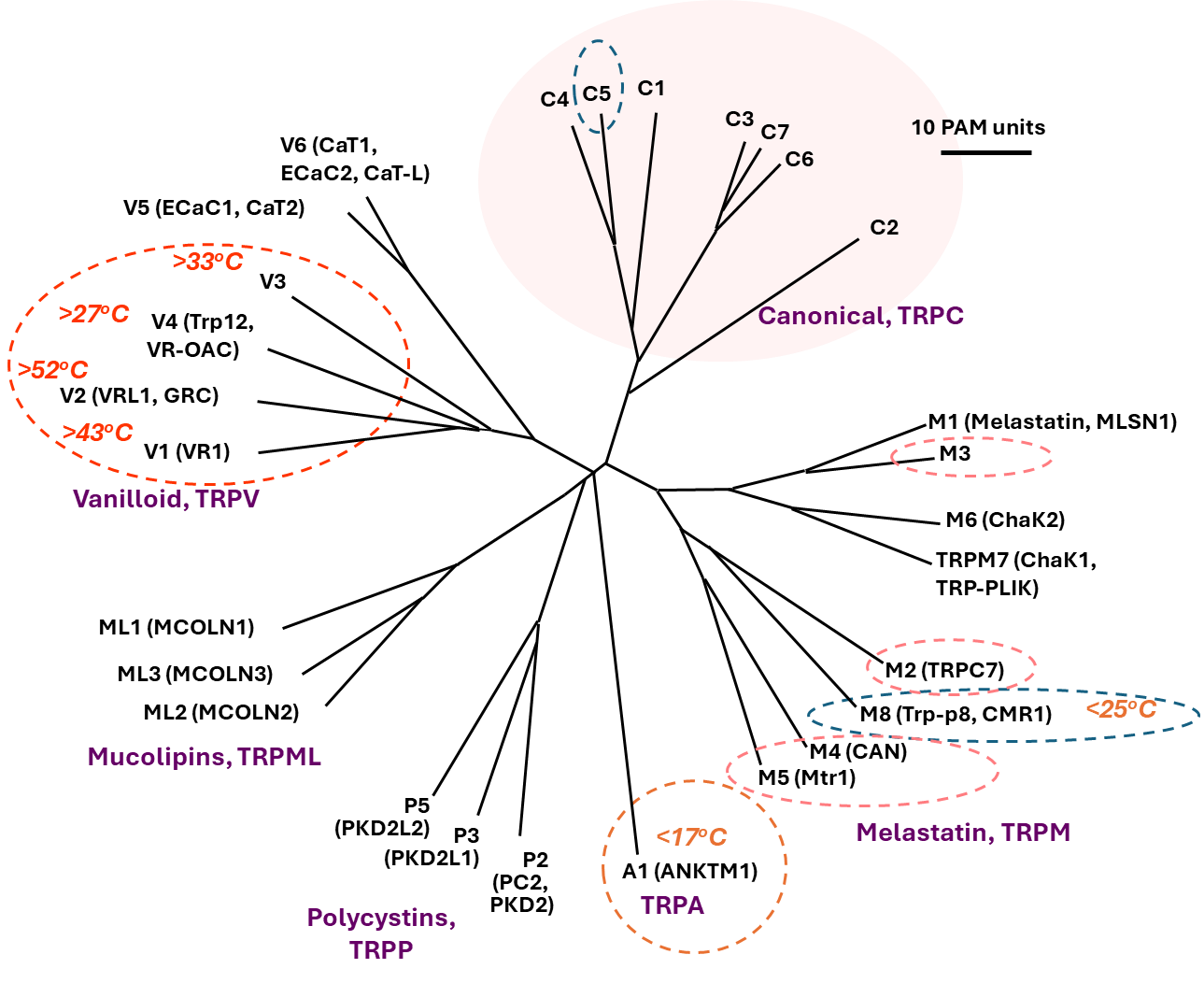
图2. 瞬时受体电位(TRP)离子通道。哺乳动物TRP超家族包含28个成员,分为六个亚家族:TRPA、TRPC、TRPM、TRPML、TRPP和TRPV。其中经典成员TRPC(粉色阴影区域)与最初在果蝇中发现的TRP蛋白进化上密切相关,该超家族亦由此得名。虚线椭圆形框标示出温度敏感型TRP通道。括号中的名称为统一命名法确立前所使用的旧称。
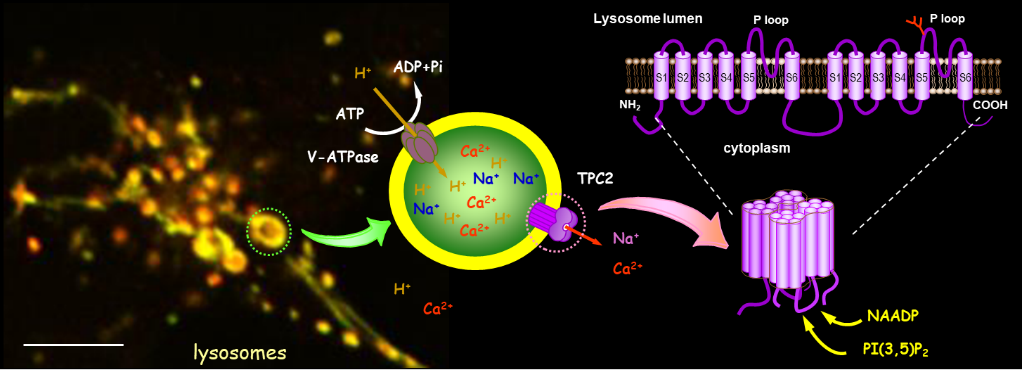
图3.双孔通道(TPCs)。双孔通道(TPC1和TPC2)表达于内体和溶酶体膜上,可响应第二信使NAADP和PI(3,5)P₂,介导这些酸性钙库中钙离子(Ca²⁺)与钠离子(Na⁺)的释放。这些通道参与多种重要生理功能,包括细胞内囊泡运输、胆固醇转运、色素生成以及病毒感染等过程。
1. Zhao, F., Xi, C., Li, J., Ren, K., Tang, Q., Liang, H., Yang, S., Zhu, M.X., and Cao, Z. Molecular determinant of low-voltage dependence of human Nav1.7 inactivation revealed by efficacy-based Nav1.7 selective inhibitor. Nat Commun. 2026, Article in Press. doi: 10.1038/s41467-026-69184-8.
2. Jeon, J., Moore, T.I., So, I., Freichel, M., Flockerzi, V., Birnbaumer, L., and Zhu, M.X. TRPC4 regulates limbic behavior and neuronal development by stabilizing dendrite branches through actomyosin-driven integrin activation. Proc Natl Acad Sci U S A. 122(33):e2511037122, 2025. doi: 10.1073/pnas.2511037122.
3. Guo, S.S., Gong, Y., Zhang, T.T., Su, X.Y., Wu, Y.J., Yan, Y.X., Cao, Y., Song, X.L., Xie, J.C., Wu, D., Jiang, Q., Li, Y., Zhao, X., Zhu, M.X., Xu, T.L., and Liu, M.G. A thalamic nucleus reuniens-lateral septum-lateral hypothalamus circuit for comorbid anxiety-like behaviors in chronic itch. Sci Adv. 10(33):eadn6272, 2024. doi: 10.1126/sciadv.adn6272.
4. Xiong, J., Luu, T.T.T., Venkatachalam, K., Du, G., and Zhu, M.X. Glutamine produces ammonium to tune lysosomal pH and regulate lysosomal function. Cells 12(1):80, 2022. https://doi.org/10.3390/cells12010080.
5. Gao, Y., Ma, R., Weng, W., Zhang, H., Wang, Y., Guo, R., Gu, X., Yang, Y., Yang, F., Zhou, A., Cheng, J., Chen, Z.Y., Zhu, M.X., and Li, Y. TRPV1 SUMOylation suppresses itch by inhibiting TRPV1 interaction with H1 receptors. Cell Rep. 39(11):110972, 2022. doi: 10.1016/j.celrep.2022.110972.
6. Tian, J.B., Yang, J., Joslin, W.C., Flockerzi, V., Prescott, S.A., Birnbaumer, L., and Zhu, M.X. TRPC4 and GIRK channels underlie neuronal coding of firing patterns that reflect Gq/11-Gi/o coincidence signals of variable strengths. Proc Natl Acad Sci U S A. 119(20):e2120870119, 2022. doi: 10.1073/pnas.2120870119.
7. Zhan, Q., Jeon, J., Li, Y., Huang, H., Xiong, J., Wang, Q., Xu, T.L., Li, Y., Ji, F.H., Du, G., and Zhu, M.X. CAMK2/CaMKII activates MLKL in short-term starvation to facilitate autophagic flux. Autophagy 18(4):726-744, 2022. doi: 10.1080/15548627.2021.1954348.
8. Wang, J.J., Liu, F., Yang, F., Wang, Y.Z., Qi, X., Li., Y., Hu, Q., Zhu, M.X., and Xu, T.L. Disruption of auto-inhibition underlies conformational signaling of ASIC1a to induce neuronal necroptosis. Nat Commun. 11(1):475, 2020. doi: 10.1038/s41467-019-13873-0.
9. Calcraft, P.J., Ruas, M., Pan, Z., Cheng, X., Arredouani, A., Hao, X., Tang, J., Rietdorf, K., Teboul, L., Chuang, K.T., Lin, P., Xiao, R., Wang, C., Zhu, Y., Lin, Y., Wyatt, C.N., Parrington, J., Ma, J., Evans, A.M., Galione, A., and Zhu, M.X. NAADP mobilizes calcium from acidic organelles through two-pore channels. Nature 459(7246):596-600, 2009. doi: 10.1038/nature08030.
10. Zhu, X., Jiang, M., Peyton, M., Boulay, G., Hurst, R., Stefani, E., and Birnbaumer, L. trp, a Novel mammalian gene family essential for agonist-activated capacitative Ca2+ entry. Cell 85(5):661-671, 1996. doi: 10.1016/s0092-8674(00)81233-7.
联系方式
地址:深圳市光明区高科创新中心
电话:+86-755-86967710
邮箱:webmaster@szbl.ac.cn
邮编:518132
Copyright © 2025 深圳湾实验室 版权所有www.szbl.ac.cn All Rights Reserved.粤ICP备19032884号 粤公网安备44031102000926号
粤公网安备44031102000926号


