
2026年1月20日,深圳湾实验室饶浪课题组与合作者在知名期刊National Science Review发表了题为In situ generation of dendritic cell vaccines in 3D printing scaffolds for cancer post-surgical therapy的研究论文。研究团队成功开发了一种基于3D生物打印技术的原位树突状细胞(DC)疫苗,可实现体内直接高效诱导预载细胞分化成熟,显著激发系统性抗肿瘤免疫以抑制肿瘤术后复发,并在前列腺癌模型中展现出优异的抗转移与“骨保护”治疗效果。这一成果成功破解了传统DC疫苗依赖复杂体外制备的转化难题,有望为个性化肿瘤术后治疗开辟更加简便、高效的新路径。
树突状细胞(DC)疫苗作为一种重要的癌症免疫疗法,在临床前和临床研究中均展现出巨大的抗肿瘤潜力。但是,传统DC疫苗需要经过单核细胞分离、诱导分化和抗原负载等多步复杂的体外培养程序。这种个性化制造的复杂性导致生产周期长达2-3周,且成本高昂,严重阻碍了其广泛的临床转化。
为解决这一挑战,研究团队设计了一种原位生成的支架DC疫苗(isDCV)。该疫苗通过3D生物打印技术,将未分化的骨髓单核细胞(BM-MNCs)、刺激因子(GM-CSF和FLT3L)以及经过X射线照射处理的个性化肿瘤裂解物(DTL)共包裹在明胶甲基丙烯酰(GelMA)水凝胶中(图1)。
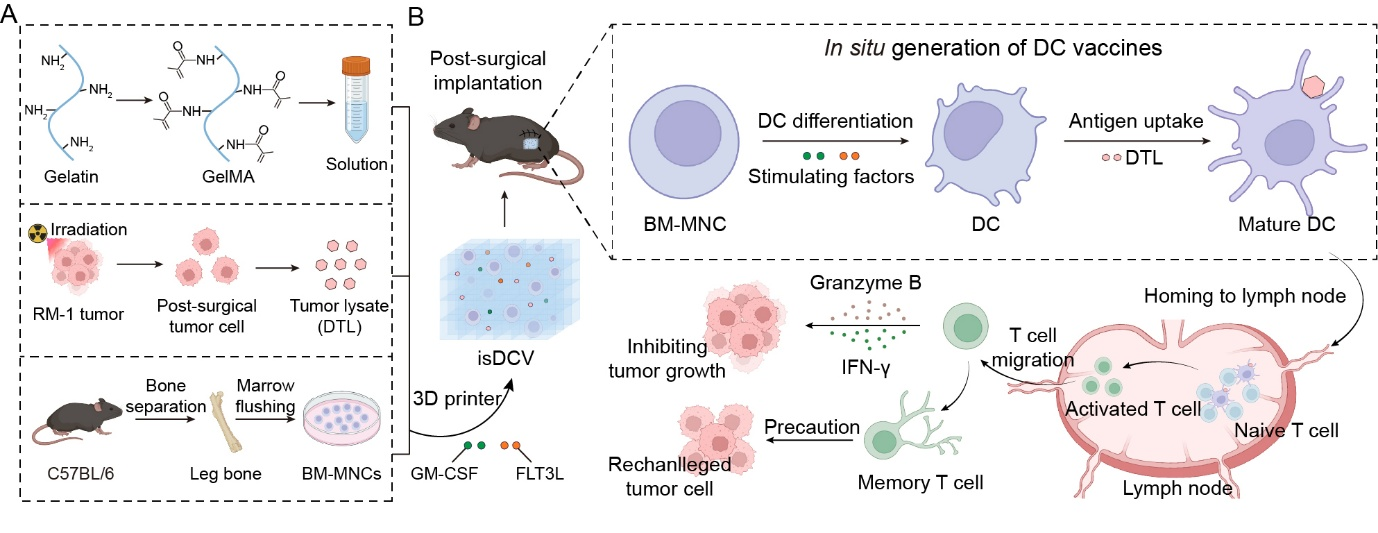
图1 isDCV的制备流程及体内抗肿瘤免疫机制示意图
研究团队首先评估了该载体系统在体内原位诱导细胞分化与成熟的能力。流式细胞术及分子生物学分析结果表明,isDCV支架植入活体内后,能够充当高效的“细胞培育工厂”。它能将预先负载于其中的BM-MNCs直接且高效地诱导分化为DCs。对水凝胶支架中的细胞进行分析发现,随着时间推移,不仅CD11c+树突状细胞的比例和绝对数量呈显著的上升趋势,其表面成熟标志物(CD86、CD80、MHC-II)的阳性表达及相关的核心转录因子(Zbtb46、Irf4、Irf8)的基因表达水平也获得明显上调。这些数据充分证实,isDCV系统能够成功实现直接在活体支架内部使预载细胞向成熟DC分化(图2)。
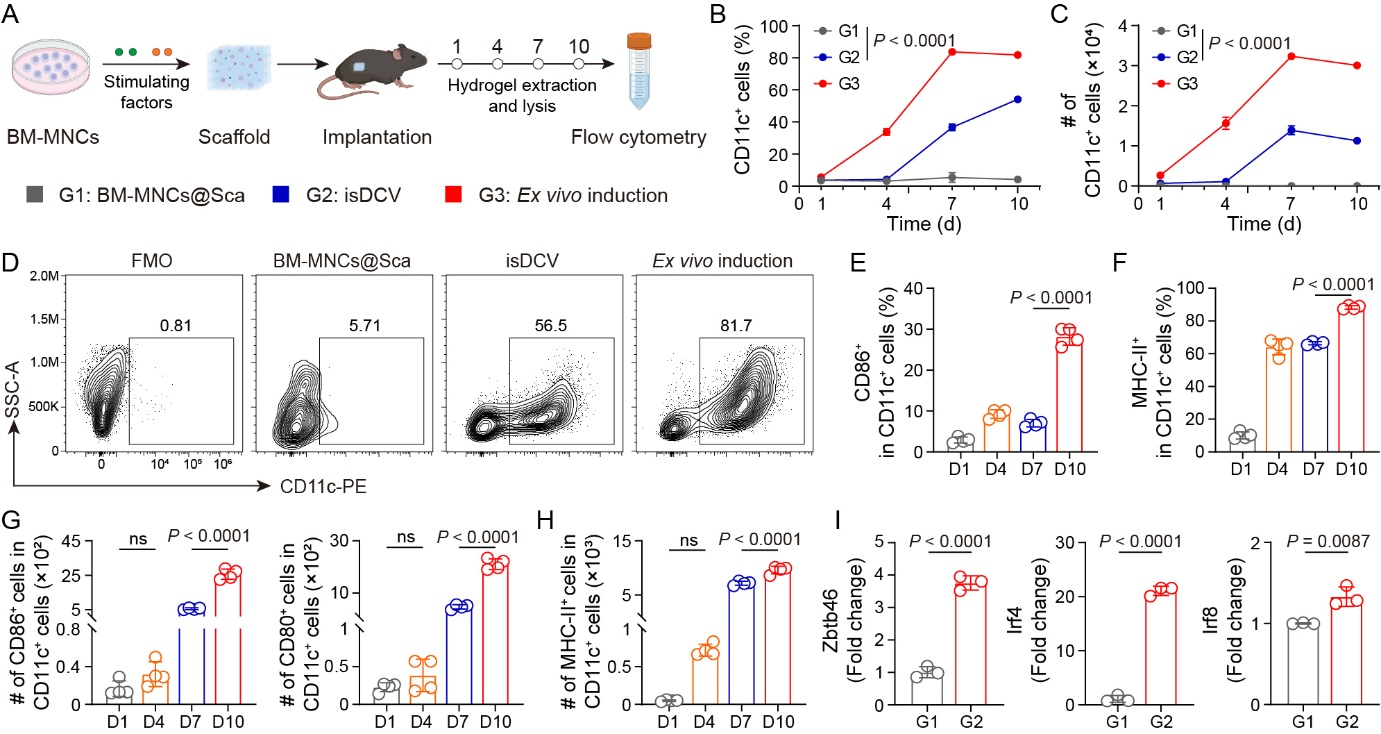
图2 isDCV支架系统在活体内原位诱导细胞分化与DC成熟的效能评估
基于isDCV能在体内高效生成成熟DCs这一关键突破,研究团队进一步在前列腺癌(RM-1)术后骨转移模型中,检验了该疫苗系统激发的系统性抗肿瘤疗效。活体生物发光成像及长期动态监测结果显示,接种isDCV的小鼠在面对肿瘤侵袭时,其骨转移灶的荧光信号受到了强烈且持久的抑制,患肢异常肿胀现象得到显著控制,中位生存期延长至55天。更为引人注目的是,Micro-CT影像学及骨体积定量数据直观地揭示了isDCV优异的“骨保护”效应:与对照组中出现的严重病理性骨质破坏与异常增生不同,接受isDCV治疗的小鼠成功抵御了肿瘤细胞对骨骼的侵袭,其患肢骨形态与骨量几乎完全维持在健康水平。这些体内疗效数据证明,isDCV不仅能激发强效的抗肿瘤免疫保护,更为预防肿瘤术后骨转移提供了一种极具转化前景的新型干预策略(图3)。
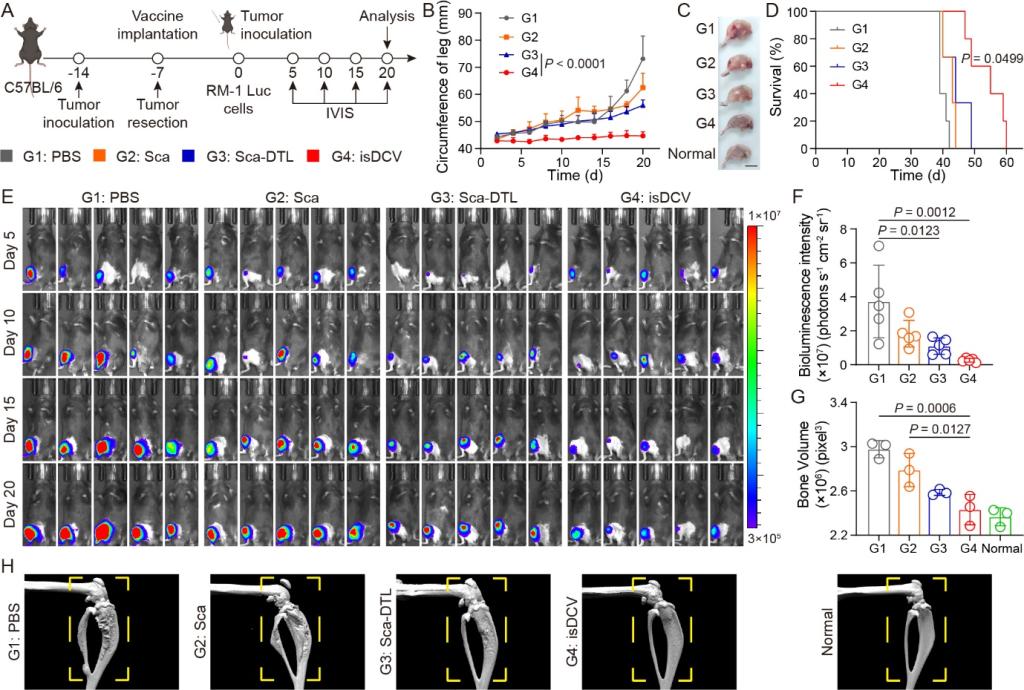
图3 isDCV在RM-1术后骨转移模型中的系统性抗肿瘤疗效
总而言之,研究团队开发的3D打印原位DC疫苗有效绕过了传统繁琐的体外细胞制备流程,成功突破了长期阻碍DC疫苗广泛临床转化的关键技术瓶颈,有望为个性化肿瘤免疫治疗提供一种简便、高效的策略。
该研究成果近日发表于知名期刊National Science Review。本文第一作者为郑州大学第一附属医院与深圳湾实验室联合培养硕士生陈乐凡、武汉大学人民医院与深圳湾实验室联合培养博士生徐阳涛与深圳湾实验室博士后胡啸;通讯作者为郑州大学第一附属医院泌尿外科李琦教授、深圳湾实验室化学生物学研究所饶浪研究员。该研究工作得到了深圳市医学研究专项基金、国家自然科学基金、广东省基础与应用基础研究基金等资助。特别感谢深圳湾实验室彭旗宇研究员团队提供小动物CT影像支持。
原文信息:
In situ generation of dendritic cell vaccines in 3D printing scaffolds for cancer post-surgical therapy
文章来源 | 饶浪课题组
编辑 | 鲍 啦
责编 | 远 山
欢迎投稿、建议 | media@szbl.ac.cn

 粤公网安备44031102000926号
粤公网安备44031102000926号